候选药物经过严格的人体内I期临床试验
发布日期:2019.09.29 16:03:00
一项研究显示,任何有前景的候选药物都必须经过严格的人体内I期临床试验。出国看病机构爱诺美康了解到,前面的讨论解释了为什么说通常在患者体内进行的药物试验才是对该药耐受性的首次真正检测,这在美国称为I期临床试验。候选药物按照不同的剂量,其中包括拟定的治疗剂量进行试验,并精确测量药物的毒性副作用。
出国看病机构爱诺美康介绍,通常这些药物试验的初始尝试剂量要远低于会导致任何明显毒性的剂量(如动物实验毒性剂量的1/10),然后在一系列患者中逐步增加剂量,直到药物水平达到开始引起不可耐受的毒性为止。这种“剂量爬坡”产生了一个值——Max耐受剂量(MTD)——用来指导下一步的治疗方案。
皮疹或短暂性恶心等副作用一般可以耐受,不会影响药物的进一步研发,然而其他一些副作用,如重度腹泻或骨髓抑制,可能是难以承受甚至是威胁生命的,以至于会促使我们迅速放弃对这些药物的进一步开发。
在I期临床试验中,像先前对动物做的药代动力学检测一样,也将运用药代动力学
测试来确定药物是否能在肿瘤细胞中达到足够的浓度并维持足够的时间。
同样,这些测试不能指示出肿瘤细胞是以何种方式应答的——这是之前描述的药效动力学的范畴。
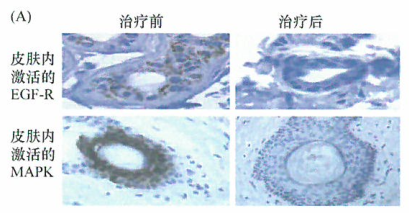
出国看病机构爱诺美康介绍,例如,图中显示的是用EGF受体阻断剂(这里显示了一个单克隆抗体和一个低分子景酪氨酸激酶抑制剂)进行治疗的药效动力学反应。为了测定患者肿瘤中EGF-R抑制剂的治疗效果,肿瘤学家以患者皮肤细胞中的EGF-R活性作为替代指标进行检测,这种方法要容秘进行得多。
文章关键词:肿瘤
一项药效动力学检测和治疗窗确定的研究,肿瘤组织中EGF-R受抑制的程度原则上可以通过药物对皮肤中EGF-R抑制的效果来评价,而且后者很容易通过小皮肤活检确定。美国看病机构爱诺美康了解到,...
下一篇:肿瘤治疗药物治疗指数研究进展一项研究报告,我们将注意力转移到药物的治疗指数上——药物影响癌组织的效率与它在正常组织内毒性的比值。美国就医机构爱诺美康了解到,显然,理想的肿瘤治疗药物应具有很高的治疗指数,大...
根据2025年ASCO年会上公布的一期KANDLELIT-001试验(NCT05067283)数据显示,新一代KRAS G12C共价抑制剂MK-1084在KRAS G12C突变的晚期结直肠癌(CRC)患者中作为单药治疗和联合治疗的一部分是安全的,并且产生了...
Vorasidenib在高度IDH突变型胶质瘤中表现出良好的安全性和疾病稳定性根据2025年神经肿瘤学会年会上公布的短期回顾性研究数据,药物Voradidenib(商品名Vorangio)在3级或4级IDH突变型胶质瘤患者群体中展现出了良好的耐受性,并且能够使病情保持稳定。这些患者因不符合3期INDIGO试验...
Dana-Farber癌症研究所获得Elaine和Eduardo Saverin基金会2000万美元的资助Elaine与Eduardo Saverin基金会向Dana-Farber癌症研究所慷慨授予2000万美元专项拨款,旨在加速转移性癌症领域的研究探索与护理服务升级。凭借这笔重要资金,该基金会成为Dana-Farber在转移性乳腺癌研究方面最大的...
什么是肺癌2期?分期和关键事实肺癌分期系统较为复杂,不过通常会综合考量肿瘤大小、淋巴结受累情况以及有无远处转移等因素。 对于非小细胞肺癌: 肿瘤较小且局限情况:若肿瘤直径小于3厘米,尚未侵犯周围重要结构,且未扩散至淋巴结,一...
FDA接受Padcev Plus Keytruda用于某些膀胱癌症患者的申请美国食品和药物管理局(FDA)已受理Lenvima(lenvatinib mesylate)联合Opdivo(nivolumab)作为术前(新辅助)治疗的补充新药申请(sNDA),并将其作为不符合卡铂化疗条件的局部进展期胰腺癌(LAPC)患者的术后...
-
 美国国家儿童医院
美国国家儿童医院 美国国家儿童医院对爱诺美康转诊资质的认证。
-
 西达赛奈医疗中心
西达赛奈医疗中心 西达赛奈医疗中心对爱诺美康转诊资质的认证
-
 皇家马斯顿医院
皇家马斯顿医院 爱诺美康与皇家马斯顿医院达成服务共识。
-
 加州大学洛杉矶分校医学中心
加州大学洛杉矶分校医学中心 加州大学洛杉矶分校医学中心(UCLA Health)与爱诺美康签署正式合作协议。
-
 丹娜法伯癌症研究院
丹娜法伯癌症研究院 丹娜法伯/布列根和妇女医院癌症中心对爱诺美康转诊资质的认证。
-
 麻省总医院(1)
麻省总医院(1) 麻省总医院对爱诺美康转诊资质的认证(NO.1页)。
-
 麻省总医院(2)
麻省总医院(2) 麻省总医院对爱诺美康转诊资质的认证(NO.2页)。
-
 辛辛那提儿童医院
辛辛那提儿童医院 辛辛那提儿童医院(美国2018-2019儿童肿瘤排名NO.1)对爱诺美康转诊资质的认证。










 MD安德森癌症中心
MD安德森癌症中心 丹娜法伯癌症研究院
丹娜法伯癌症研究院 辛辛那提儿童医院
辛辛那提儿童医院 克利夫兰医学中心
克利夫兰医学中心 纪念斯隆凯特琳癌症中心
纪念斯隆凯特琳癌症中心 Mayo Clinic 梅奥诊所
Mayo Clinic 梅奥诊所 麻省总医院
麻省总医院 肺癌
肺癌 乳腺癌
乳腺癌 结肠癌
结肠癌 淋巴瘤
淋巴瘤 肉瘤
肉瘤 宫颈癌
宫颈癌 卵巢癌
卵巢癌 脑瘤
脑瘤 奥希替尼耐药,只剩3个月生存期,“笨办法”让我再次用上肺癌靶向药
奥希替尼耐药,只剩3个月生存期,“笨办法”让我再次用上肺癌靶向药 晚期乳腺癌生命只剩6个月,她能逆袭吗?
晚期乳腺癌生命只剩6个月,她能逆袭吗? 为了多活10年,我带妈妈去美国治疗淋巴瘤
为了多活10年,我带妈妈去美国治疗淋巴瘤 不认命 我带父亲去麻省总医院看肺癌
不认命 我带父亲去麻省总医院看肺癌 成功可以复制,美国这家医院再次治好晚期乳腺癌
成功可以复制,美国这家医院再次治好晚期乳腺癌 肿瘤复发,我去美国看病的日子
肿瘤复发,我去美国看病的日子 北京淋巴瘤患者赴美治疗后,体内癌细胞完全消失
北京淋巴瘤患者赴美治疗后,体内癌细胞完全消失 疫情之下,美国肿瘤专家弛缓晚期肠癌患者
疫情之下,美国肿瘤专家弛缓晚期肠癌患者
